1. 臨床試驗(yàn)要求
根據(jù)《醫(yī)療器械監(jiān)督管理?xiàng)l例》規(guī)定���,第I類(lèi)醫(yī)療器械實(shí)行產(chǎn)品備案管理���,不需要進(jìn)行臨床試驗(yàn)���。第II/III類(lèi)醫(yī)療器械注冊(cè)時(shí)��,應(yīng)當(dāng)進(jìn)行是否需要臨床評(píng)價(jià)的評(píng)估���。對(duì)于不能免于臨床評(píng)價(jià)的產(chǎn)品需按照臨床評(píng)價(jià)的要求,進(jìn)行同品種比對(duì)或臨床試驗(yàn)�。
2. 服務(wù)內(nèi)容
1.為客戶(hù)確定是否需要進(jìn)行臨床試驗(yàn),如需要����,提供臨床試驗(yàn)方案的起草服務(wù)
2.提供臨床試驗(yàn)基地的選擇及聯(lián)絡(luò)接洽相關(guān)的服務(wù)。
3.提供臨床試驗(yàn)方案���、CRF表格起草及咨詢(xún)的服務(wù)�����。
4.提供臨床試驗(yàn)批件提交���、備案、不良事件報(bào)告等服務(wù)�����。
5.提供整個(gè)臨床試驗(yàn)開(kāi)啟至關(guān)閉全程跟蹤并取得報(bào)告的服務(wù)��。
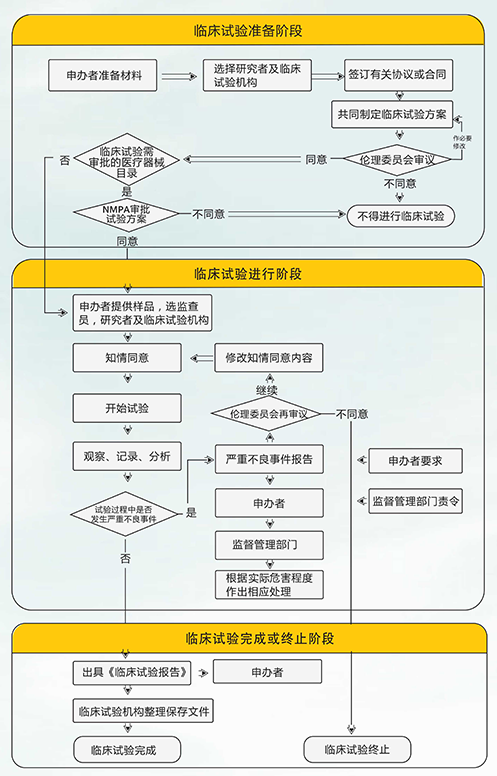
3. 服務(wù)流程

 18957164022
18957164022 
 18957164022
18957164022